NOMENCLATURA
LOS COMPUESTOS
No son frutos de combinaciones al azar de los elementos de la Tabla Periódica, sino que son el resultado de la combinación, en unas determinadas proporciones, de elementos que guardan entre sí una cierta “afinidad”. Estas limitaciones vienen prefijadas por la capacidad de combinación o valencia de los elementos que, a su vez, es función de la estructura electrónica de los átomos implicados.
En química, el grupo de algunas sustancias compuestas que poseen propiedades químicas semejantes, denominadas propiedades funcionales, recibe el nombre de función química. Cuando un determinado compuesto posee características como acidez o basicidad, solubilidad en agua, reactividad de acuerdo con determinada función química, se dice que este pertenece a esta función química. Las funciones químicas son divididas de acuerdo con la división clásica de la química.
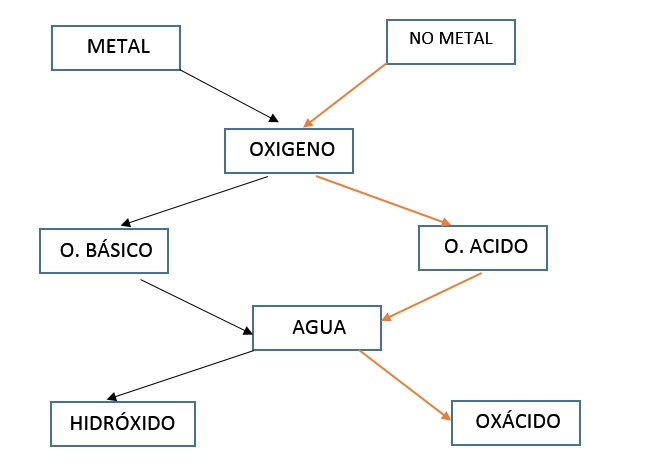
Existen cuatro tipos de función inorgánica: óxido, ácido, base y sal. El criterio de clasificación de una sustancia en una de esas funciones es el tipo de iones que se forman cuando ella es disuelta en agua.
NOMENCLATURA TRADICIONAL
En un sentido amplio, nomenclatura química son las reglas y regulaciones que rigen la designación (la identificación o el nombre) de las sustancias químicas.
Como punto inicial para su estudio es necesario distinguir primero entre compuestos orgánicos e inorgánicos.
Los compuestos orgánicos son los que contienen carbono, comúnmente enlazado con hidrógeno, oxígeno, boro, nitrógeno, azufre y algunos halógenos. El resto de los compuestos se clasifican como compuestos inorgánicos. Éstos se nombran según las reglas establecidas por la IUPAC.
Nomenclatura en química inorgánica
Los compuestos inorgánicos se clasifican según la función química que contengan y por el número de elementos químicos que los forman, con reglas de nomenclatura particulares para cada grupo.
Una función química es la tendencia de una sustancia a reaccionar de manera semejante en presencia de otra. Por ejemplo, los compuestos ácidos tienen propiedades características de la función ácido, debido a que todos ellos tienen el ion H+1; y las bases tienen propiedades características de este grupo debido al ion (OH)-1 presente en estas moléculas
Cuando el elemento solo tiene una valencia, simplemente se coloca el nombre del elemento precedido de la sílaba “de” o bien se termina el nombre del elemento con el sufijo –ico.
Oxido de Nombre del Elemento
K2O, óxido de potasio u óxido potásico
Cuando tiene dos valencias diferentes se usan los sufijos -oso e -ico.
Oxido ________ Oso
Oxido ________ Ico
Cuando el elemento usa la valencia menor: Fe+2 +3
FeO, Hierro con la valencia 2, (estado de oxidación +2), óxido ferroso
Fe2O3 Hierro con valencia 3, (estado de oxidación +3), óxido férrico
Cuando tiene tres distintas valencias se usan los prefijos y sufijos.
Oxido Hipo ________ Oso
Oxido ________ Oso
Oxido ________ Ico
PO, fósforo con la valencia 1, (estado de oxidación +1), óxido hipofosforoso
P2O3 fósforo con valencia 3, (estado de oxidación +3), óxido fosforoso
P2O5, fósforo con valencia 5, (estado de oxidación +5), óxido fosfórico
Cuando tiene cuatro valencias diferentes se usan los prefijos y sufijos
Oxido Hipo________ Oso (para la valencia más pequeña)
Oxido ________ Oso (para la valencia pequeña)
Oxido ________ Ico (para la valencia grande)
Oxido Per ________ Ico (para la valencia más grande)
ClO (estado de oxidación +1), Oxido Hipo Cloroso
Cl2O3 (estado de oxidación +3), Oxido Cloroso
Cl2O5 (estado de oxidación +5), Oxido Clorico
Cl2O7 (estado de oxidación +7), Oxido Per Clorico
NOMENCLATURA STOCK-WERNER.
Se escribe "óxido de" y el nombre del elemento metálico. Se escribe la valencia, en números romanos y entre paréntesis, pero sólo cuando presenta dos o más Valencias.
Oxido de Nombre del Elemento (Numero de Oxidación del Elemento en Números Romanos)
Fe+2 +3
FeO, Se Nombra: Óxido de Hierro (II)
Fe2O3 Se Nombra: Óxido de Hierro (III)
Se escribe "óxido de" y el nombre del elemento metálico. Se escribe la valencia, en números romanos y entre paréntesis, pero sólo cuando presenta dos o más Valencias.
Oxido de Nombre del Elemento (Numero de Oxidación del Elemento en Números Romanos)
Fe+2 +3
FeO, Se Nombra: Óxido de Hierro (II)
Fe2O3 Se Nombra: Óxido de Hierro (III)
ACTIVIDADES
REALICE LA SIGUIENTE EVALUACIÓN Y PRESENTE LA RESPUESTA AL DOCENTE
B) oxido perclorico
C) acido perclorico
D) oxido hipocloroso
B) C(OH)2
C) HCO
D) HCO2
B) CuO3
C) CuO
D) Cu2O
B) oxidopermanganoso
C) oxido hipopermanganoso
D) Oxido permanganico
B) pentoxido de dicloro
C) dioxido de pentacloro
B) un metal + agua
C) un no metal + agua
D) un elemento metalico + oxigeno
B) metal + agua
C) un no metal + oxigeno
D) metal + oxigeno
B) oxido basico + agua
C) no metal + agua
D) un oxido acido + agua
B) con cualquier metal + hidrogeno
C) con la combinacion de un elemento metalico del grupo VI y VII + hidrogeno
D) con un no metal + hidrogeno
B) acido hiposulfuroso
C) acido sulfurico
D) acido sulfhidrico
B) H2Br
C) BrH
D) HBr
B) H2SO2
C) H2SO3
D) H2SO3
B) acido clororso
C) acido percloroso
D) acido clorico
B) acido pernitrico
C) acido nitroso
D) acido hiponitroso
B) acido permanganoso
C) acido hipomanganico
D) acido manganico
- 1. en la nomenclatura tradicional la siguiente formula Cl2O7 corresponde a
B) oxido perclorico
C) acido perclorico
D) oxido hipocloroso
- 2. con la siguiente reaccionobtengo CO2+ H2O→
B) C(OH)2
C) HCO
D) HCO2
- 3. la formula deloxido cuprico es
B) CuO3
C) CuO
D) Cu2O
- 4. Mn2O7
B) oxidopermanganoso
C) oxido hipopermanganoso
D) Oxido permanganico
- 5. en la nomenclatura sistematica en siguiente compuesto se llama Cl2O5
B) pentoxido de dicloro
C) dioxido de pentacloro
- 6. los oxidos basicos se formana apartir de
B) un metal + agua
C) un no metal + agua
D) un elemento metalico + oxigeno
- 7. los oxidos acidos se forman a apartir de
B) metal + agua
C) un no metal + oxigeno
D) metal + oxigeno
- 8. los acidos oxacidos se forman a partir de
B) oxido basico + agua
C) no metal + agua
D) un oxido acido + agua
- 9. los acidos hidracidos se forman por la union
B) con cualquier metal + hidrogeno
C) con la combinacion de un elemento metalico del grupo VI y VII + hidrogeno
D) con un no metal + hidrogeno
- 10. el siguiente acido se llama H2S
B) acido hiposulfuroso
C) acido sulfurico
D) acido sulfhidrico
- 11. el acido bromhidrico corresponde a la formula
B) H2Br
C) BrH
D) HBr
- 12. el SO3+H2O→
B) H2SO2
C) H2SO3
D) H2SO3
- 13. HClO4 corresponde a la formula de
B) acido clororso
C) acido percloroso
D) acido clorico
- 14. HNO3 corresponde a la formula del
B) acido pernitrico
C) acido nitroso
D) acido hiponitroso
- 15. el H2Mn2O8 corresponde al
B) acido permanganoso
C) acido hipomanganico
D) acido manganico